-
Khuyến cáo mới nhất của CDC về 5 loại vắcxin phổ biến nhất hiện nay
-
Khuyến cáo mới nhất của CDC về 5 loại vắcxin phổ biến nhất hiện nay
Do không đủ tiêu chuẩn sử dụng Cục Quản lý Dược vừa yêu cầu đình chỉ lưu hành Bột pha hỗn dịch uống Batimin 125 do Công ty cổ phần dược phẩm và sinh học y tế sản xuất.
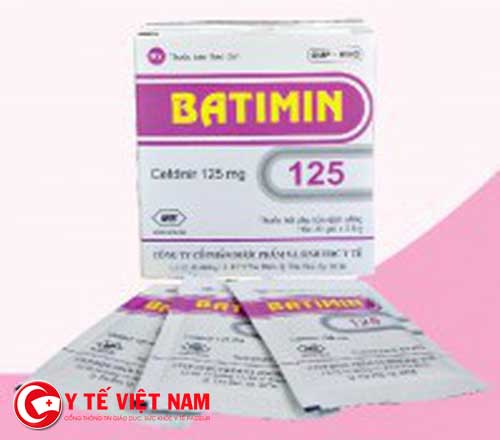
Quyết định thu hồi thuốc thuốc bột pha hỗn dịch uống Batimin 125
Đỉnh chỉ lưu hành thuốc bột pha hỗn dịch uống Batimin
Theo tin tức Y tế cập nhật thì mới đây 125 Cục Quản lý Dược – Bộ Y tế đã có công văn số 19362/QLD- CL gửi Sở Y tế các tỉnh, thành phố thông báo đình chỉ lưu hành Bột pha hỗn dịch uống Batimin 125 của Công ty cổ phần dược phẩm và sinh học y tế vì kém chất lượng. Quyết định này được căn cứ vào kết quả kiểm nghiệm của Viện Kiểm nghiệm thuốc Trung ương, thuốc Bột pha hỗn dịch uống Batimin 125 (Cefdinir 125mg) SĐK: VD-25824-16, số lô: 0417; NSX: 08/11/2017; HD: 8/11/2020 bị đình chỉ lưu hành và thu hồi là thuốc không đạt tiêu chuẩn chất lượng về chỉ tiêu tính chất và định lượng.
Cũng trong văn bản này Cục Quản lý Dược yêu cầu Công ty cổ phần dược phẩm và sinh học y tế phối hợp với nhà phân phối thuốc phải khẩn trương gửi thông báo thu hồi tới các cơ sở bán buôn, bán lẻ, sử dụng Bột pha hỗn dịch uông Batimin 125 SĐK: VD-25824-16, số lô: 0417; NSX: 08/11/2017; HD: 8/11/2020 và tiến hành thu hồi toàn bộ lô thuốc không đạt tiêu chuẩn chất lượng nêu trên để đảm bảo thuốc không gây ảnh hưởng đến sức khỏe người dùng.
Công ty cổ phần dược phẩm và sinh học y tế phải gửi báo cáo thu hồi về Cục Quản lý Dược trong vòng 18 ngày kể từ ngày ký công văn này, hồ sơ thu hồi bao gồm số lượng sản xuất, số lượng phân phối, ngày sản xuất, số lượng thu hồi, các bằng chứng về việc thu hồi tại các cơ sở bán buôn, bán lẻ, sử dụng thuốc đã mua theo quy định tại Thông tư số 11/2018/TT-BYT ngày 4/5/2018 của Bộ Y tế quy định về chất lượng thuốc, nguyên liệu làm thuốc.
Ngoài ra, Cục Quản lý Dược đề nghị Sở Y tế các tỉnh thành phố trực thuộc Trung ương, Y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc thu hồi lô thuốc không đạt chất lượng nêu trên, kiểm tra và giám sát các đơn vị thực hiện thông báo này, xử lý những đơn vị vi phạm theo quy định hiện hành báo cáo về Cục Quản lý Dược và các cơ quan chức năng có liên quan.
Nguồn: ytevietnam.net.vn